LAS ENFERMEDADES TRANSMITIDAS POR LOS ALIMENTOS (Parte 9)
Más de una vez Ud. habrá dicho: “Debe ser algo que comí”,
“Algo me cayó mal” ó “Me dio un ataque de hígado”, luego de haber estado con
diarreas, vómitos, dolor de cabeza ó cólicos. Lo más probable es que sí; algo
le cayó mal, y no precisamente lo que comió, sino, lo que no vio al ingerir ese
alimento, ya que éste tenía el aspecto de estar sano, pero...no fue así.- Lo
que usted sufrió es una Enfermedad Transmitida por Alimentos (ETA)
Criptosporidiosis (cie-10 a07.2)
Es
una enfermedad emergente. Los primeros casos fueron descritos en 1976 y desde
mediados de la década del '80, han ocurrido epidemias transmitidas por agua en
distintas comunidades. Cryptosporidium
parvum,
coccidio del subreino Protozoa es el causante. Se han identificado dos
genotipos: el 1 (o humano) exclusivamente del hombre y de los primates no
humanos y el 2 en el ganado y el hombre, lo que podría indicar que serían dos
especies con ciclos exclusivos de transmisión. La dosis infectante es baja
(hasta un quiste) y en promedio 132.
Tiene
distribución universal. La mayor ocurrencia se observa en primavera lo cual
estaría relacionado con el aumento de las precipitaciones y la posibilidad de
contaminación de las fuentes de agua. Ha sido encontrado en el 87 % de las
muestras de agua en los Estados Unidos y Canadá. La
infección se adquiere por vía oral y es de origen fecal. Puede proceder de
personas infectadas que contaminan a través de manos, contaminación oro-anal,
aguas, hortalizas, etc. La infección también puede transmitirse por materia
fecal de animales que sufran la parasitosis. Los animales reservorios son
muchos, por lo cual se considera una zoonosis frecuente. Los ooquistes son muy
resistentes a las condiciones del medio ambiente y pueden sobrevivir en el
suelo por varios meses.
Pueden resistir
algunos desinfectantes comunes, pero pierden su viabilidad con la
congelación y la ebullición. Se considera la quinta causa de diarrea en niños
inmunocompetentes y la prevalencia en la población infantil ha variado de 2% a
30% de acuerdo a los países y a las condiciones higiénicas de las poblaciones
estudiadas.
En
Colombia se ha encontrado 4% de positividad en niños con diarrea en estudios
basados en el examen directo con coloración ácido-resistente, mientras que en
México, donde utilizaron inmunofluorescencia con anticuerpos monoclonales,
encontraron frecuencias de 9 a 30%. En población general se presentan ocasionalmente
brotes o epidemias, debidas a contaminación alimentaria y la incidencia tiene
variaciones estacionales o de acuerdo al clima, como se comprobó en Costa
Rica, en donde la frecuencia en niños con diarrea aumentó de 4% a 15% entre
mayo y agosto, la época caliente y lluviosa. Se considera una de las causas de
la diarrea de los viajeros.
Con
estudios seroepidemiológicos en la población, se detectan anticuerpos y se han
encontrado frecuencias de 25% a 35% en Estados Unidos y de más de 50% en
América Latina y en China. La
relación epidemiológica más importante es que se ha encontrado en portadores de VIH y
en pacientes con SIDA. En ambos casos el parásito se comporta como un agente
invasor oportunista. Se calcula que en países desarrollados los pacientes VIH
positivos son portadores del parásito entre 10% y 15% y en países en desarrollo
entre el 30% y el 50%. En pacientes con SIDA en Colombia, el 45.3% de los que
tenían diarrea fueron positivos para Cryptosporidium en materia fecal y en
Venezuela el 41.3%. En contraste, sólo de 4% a 5% fueron positivos en casos
similares de Estados Unidos.
En
el año 2000 el número de personas infectadas por VIH en el mundo era de 38
millones y han llegado casi a 40 millones a finales de 2014. Estas cifras
alarmantes, que aumentan permanentemente, hacen necesario que se establezcan
medidas de control para los agentes oportunistas que ya son más de 100. En pacientes inmunocompetentes la
diarrea generalmente es autolimitada y no requiere tratamiento. El problema
grave de la diarrea se presenta en los inmunosuprimidos.
El
reservorio primario está constituido por el ganado bovino y animales domésticos
y el hombre. La transmisión es por contaminación fecal del agua y los alimentos
(vegetales, frutas, leche no pasteurizada), también ocurre de persona a persona
y de animales al hombre. Los quistes eliminados son infectantes y se mantienen
durante 2-6 meses. Han
sido comunicados numerosos brotes que afectaron 415.000 personas desde 1984. El
más importante ocurrió en Milwaukee (Wisconsin, Estados Unidos) con 403.000
personas con diarrea. La modificación del estándar de turbidez del agua potable
(Menos de 0,17 unidades nefelométricas), sin embargo, no impidió el brote de
Las Vegas.

Un
siglo después de su descubrimiento y después de casi tres décadas de intensas
investigaciones, Cryptosporidium sigue siendo, en muchos aspectos, un enigma.
Perteneciente al phylum Apicomplexa, posee como otros coccidios entéricos de
vertebrados un ciclo de vida monoxeno que se completa primariamente en el
tracto gastrointestinal de un solo huésped. Sin
embargo, posee características únicas que lo distinguen de otros coccidios.

La localización peculiar dentro de la célula huésped, intracelular pero extracitoplasmática, que confina los estadios de desarrollo endógeno a la superficie apical de las células epiteliales; la unión del parásito a la célula huésped a través de una organela multimembranosa en la base de la vacuola parasitófora que facilita la incorporación de nutrientes desde la célula huésped; la presencia de dos tipos morfofuncionales de ooquistes, los de paredes gruesas que son excretados, y los de paredes delgadas, responsables de la iniciación del ciclo autoinfectivo en el huésped infectado; el tamaño pequeño de los ooquistes que carecen de estructuras morfológicas tales como micrópilo, esporoquistes y gránulos polares y, finalmente la insensibilidad a todos los agentes anticoccidiales probados.
La localización peculiar dentro de la célula huésped, intracelular pero extracitoplasmática, que confina los estadios de desarrollo endógeno a la superficie apical de las células epiteliales; la unión del parásito a la célula huésped a través de una organela multimembranosa en la base de la vacuola parasitófora que facilita la incorporación de nutrientes desde la célula huésped; la presencia de dos tipos morfofuncionales de ooquistes, los de paredes gruesas que son excretados, y los de paredes delgadas, responsables de la iniciación del ciclo autoinfectivo en el huésped infectado; el tamaño pequeño de los ooquistes que carecen de estructuras morfológicas tales como micrópilo, esporoquistes y gránulos polares y, finalmente la insensibilidad a todos los agentes anticoccidiales probados.
Los
coccidios del género Cryptosporidium tienen un ciclo de vida monoxeno
pues todas las etapas de su desarrollo (sexual y asexual) se completan dentro
del tracto gastrointestinal de un único huésped. Presentan un estadio exógeno
que corresponde a los ooquistes esporulados excretados por las heces de los
huéspedes infectados, u otros materiales biológicos como las secreciones respiratorias.
El diámetro de cada ooquiste varía entre 4 y 6 μm. La fase endógena del ciclo
comienza una vez que el huésped apropiado ingiere (o inhala) los ooquistes que
contienen cuatro estadios haploides o esporozoítos, los cuales escapan a través
de una fisura que se abre en la pared del ooquiste. Al parecer las
fluctuaciones de pH en el tracto gastrointestinal, las sales biliares, las
enzimas pancreáticas y la temperatura favorecen el desenquistamiento,
probablemente, a causa del aumento de la permeabilidad de la pared del ooquiste,
la movilidad de los esporozoítos dentro del ooquiste y la consecuente
exposición de receptores.
El esporozoíto se adhiere a receptores de la membrana apical de la célula epitelial del huésped mediante diversos ligandos, GP900, P23, CP47, entre otros. Este proceso induce la reorganización del citoesqueleto de actina y la protrusión de la membrana de la célula huésped alrededor del esporozoíto para formar una vacuola parasitófora, donde el microorganismo permanece en posición intracelular pero extracitoplasmática.
El esporozoíto se adhiere a receptores de la membrana apical de la célula epitelial del huésped mediante diversos ligandos, GP900, P23, CP47, entre otros. Este proceso induce la reorganización del citoesqueleto de actina y la protrusión de la membrana de la célula huésped alrededor del esporozoíto para formar una vacuola parasitófora, donde el microorganismo permanece en posición intracelular pero extracitoplasmática.
Dentro de la
vacuola, el parásito, que en este estadio recibe el nombre de trofozoíto,
comienza un ciclo de multiplicación asexual (esquizogonia o merogonia) y luego
continúa con una multiplicación sexual (gametogonia). Durante el ciclo de
proliferación asexual se forman merontes de los cuales emergen merozoítos
capaces de infectar otras células del huésped, en las que iniciarán otra
merogonia o, alternativamente, una gametogonia para diferenciarse en estadios
sexuales llamados gamontes (gametocitos). Durante la gametogénesis, los gametocitos
masculinos liberan varias microgametas, mientras que los gametocitos femeninos
se diferencian en una única macrogameta.
Luego de la fertilización el estadio diploide resultante (zigoto) sufre meiosis, mecanismo que restaura el estado haploide. A partir de aquí se inicia el proceso de esporogonia en el cual el zigoto sufre uno o más ciclos de división mitótica para formar un ooquiste que contiene los esporozoítos infectivos. Si bien se asume que la localización normal en un huésped inmunocompetente es el tracto gastrointestinal, en individuos inmunocomprometidos se han descripto fases extraintestinales en vías aéreas, árbol biliar, hígado, vejiga y páncreas.
Luego de la fertilización el estadio diploide resultante (zigoto) sufre meiosis, mecanismo que restaura el estado haploide. A partir de aquí se inicia el proceso de esporogonia en el cual el zigoto sufre uno o más ciclos de división mitótica para formar un ooquiste que contiene los esporozoítos infectivos. Si bien se asume que la localización normal en un huésped inmunocompetente es el tracto gastrointestinal, en individuos inmunocomprometidos se han descripto fases extraintestinales en vías aéreas, árbol biliar, hígado, vejiga y páncreas.
Cryptosporidium
es un patógeno entérico que desencadena una enfermedad diarreica cuya
morbilidad y mortalidad son significativas tanto para los seres humanos como
para los animales. El desarrollo de nuevas técnicas moleculares ha permitido
identificar a los genotipos C. hominis y C. parvum como aquellos que con mayor
prevalencia infectan al hombre. Las rutas de transmisión son múltiples (persona
a persona, animales a personas, agua, alimentos, aire) y la enfermedad puede
afectar a individuos inmunocomprometidos o no. Es un microorganismo emergente
cosmopolita cuya aparición no está limitada a ninguna región geográfica o al
grado de desarrollo tecnológico de la misma.
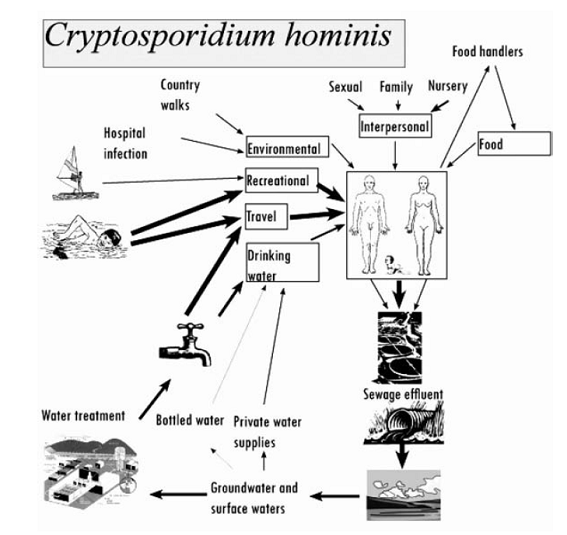
Los procesos de urbanización
acelerados, la expansión de la pobreza, las migraciones no controladas de gran número
de refugiados, la facilidad y rapidez en los desplazamientos, el movimiento
creciente de animales y de productos de origen animal, la falta de saneamiento ambiental,
son algunos de los factores que, sumados a la escasez de normas legales
regulatorias, han posibilitado la dispersión de la enfermedad. La resistencia a
los antibióticos incrementa las tasas de morbilidad y mortalidad y los gastos
de atención médica asociados con el control de brotes epidémicos. La
criptosporidiosis, entonces, representa una amenaza de alcance mundial que
exige una respuesta coordinada de los servicios de salud pública de todos los
países.
Los
quistes ingeridos se localizan en el tubo digestivo (desde la faringe al recto)
con mayor frecuencia en el intestino delgado (yeyuno). Se ubican en el
glicocálix del enterocito donde se desenquistan y cada uno elimina cuatro
esporozoítos que invaden las células epiteliales. Allí cumplen un ciclo
asexuado y otro sexuado que resulta en el ooquiste infectante eliminado a la
luz intestinal. El parásito en las microvellosidades determina la malabsorción
de nutrientes y la retención de agua en la luz intestinal lo que desencadena la
diarrea osmótica. Además es la causa del edema y la atrofia de las vellosidades
lo que resulta en una disminución de la superficie de absorción. Las heces
humanas son infectantes a partir de los 5 - 21 días de la infección.
El
período de incubación es de 1 a 21 días (promedio 7). Cursa con una diarrea
aguda secretora (puede ser mayor de 3 litros/día) con importante pérdida de
electrolitos, dolor abdominal difuso, borborigmos, náuseas, vómitos, hiporexia
y pérdida de peso. Las heces son líquidas, abundantes, oscuras, malolientes y
en un promedio de 6 / día. En las personas inmunocompetentes la enfermedad dura
3-27 días (se autolimita) y en los inmunocomprometidos mas de 1 mes, pudiendo
llevar a la caquexia y la muerte.
Las
lesiones histológicas asociadas con la criptosporidiosis intestinal no son
características. El contacto inicial entre el parásito y el glicocálix de la
célula huésped, produce un acortamiento o ausencia de las microvellosidades, con
atrofia y aumento de tamaño de la cripta. Se observa en la mucosa y hasta la
lámina propia un infiltrado moderado de células mononucleares. El
yeyuno es la localización intestinal en donde existe mayor infección. Se ha
encontrado diseminación en pacientes inmunosuprimidos, principalmente con SIDA,
a faringe, esófago, estómago, duodeno, ileum, colédoco, apéndice, colon, recto
y pulmones, en cuyo caso pueden encontrarse los ooquistes en el esputo.
En
las personas inmunocompetentes, el período de incubación varía entre 3 y 12
días. La sintomatología puede fluctuar entre la sensación de indigestión y un
cuadro de enteritis con diarrea de tipo agudo o crónico. Algunas personas pueden
tenerla infección totalmente asintomática. En
otras aparece la diarrea pero la infección se autolimita. Algunos autores la
asocian con el síndrome conocido como diarrea del viajero. La diarrea
generalmente es acuosa, sin moco ni sangre, la mayoría de las veces sin
leucocitos. Se presenta con 5 a 10 episodios diarreicos al día, después de un
tiempo puede seguirle la constipación. En niños con diarrea intensa o crónica,
se puede asociar a deshidratación.
Los
pacientes se quejan de dolores abdominales, ocasionalmente fiebre, cefalea,
anorexia, vómito y pérdida de peso. Generalmente la enfermedad se autolimita a
10-14 días. En una cuarta parte de los pacientes puede llegar a más de un mes.
La mayoría de los casos no requieren tratamiento antidiarreico. Los parásitos
desaparecen entre 4 y 6 semanas.
En
los pacientes con SIDA, además de la localización intestinal, se ha encontrado
diseminación con complicación pulmonar. Causa una neumonía intersticial con
intensa tos seca y sibilancias. Se han informado casos de colecistitis, con
colestasis, fiebre, dolor abdominal y marcada pérdida de peso. Se han comunicado
casos de pancreatitis, laringotraqueítis y sinusitis. La enfermedad es más
frecuente en los pacientes con SIDA, pero también ocurre en otras
inmunodeficiencias como hipogammaglobulinemia, terapia inmunosupresora,
desnutrición, leucemia, linfoma y otros defectos de la inmunidad.

En
los pacientes con deficiencias inmunes, los síntomas son más intensos y de
larga duración. La diarrea es crónica y ocurre una enfermedad debilitante con
malestar, anorexia y fiebre. Hay pérdida de líquidos y electrólitos que pueden
causar enfermedad grave o muerte por deshidratación.
El
diagnóstico de la criptosporidiosis se hace por el hallazgo de ooquistes en las
materias fecales o en material obtenido del duodeno por la cuerda de Beal
(Entero tests). En
las preparaciones con solución salina y lugol se pueden observar unas
estructuras redondeadas u ovoides de pared definida, como "huecos
vacíos", de tamaño uniforme, refringentes, algunas veces con estructuras
granulares internas, que no son fáciles de identificar. La técnica más precisa
es la coloración por el método de Ziehl-Neelsen modificado, sin utilizar el
calentamiento de la placa. Se observan los ooquistes ácido-resistentes, de
color rojo brillante sobre fondo azul.
En algunos se ven unos corpúsculos internos que corresponden a los esporozoítos. Otras coloraciones que se utilizan son Kinyoun y Giemsa. Para concentrar ooquistes de Cryptosporidium se realizan las técnicas de Ritchie modificada que usa formol-éter y la de Sheather que es una flotación con azúcar. Ambas son similares en efectividad. Es necesario tener precaución en la manipulación de muestras de pacientes con SIDA.
En algunos se ven unos corpúsculos internos que corresponden a los esporozoítos. Otras coloraciones que se utilizan son Kinyoun y Giemsa. Para concentrar ooquistes de Cryptosporidium se realizan las técnicas de Ritchie modificada que usa formol-éter y la de Sheather que es una flotación con azúcar. Ambas son similares en efectividad. Es necesario tener precaución en la manipulación de muestras de pacientes con SIDA.
La
identificación de los ooquistes también se hace con inmunofluorescencia
directa, para la cual hay estuches comerciales. Existen también estuches para
identificar antígenos específicos de Cryptosporidium por métodos
inmunoenzimáticos. Se
han comparado los 3 métodos diagnósticos más utilizados: visualización de los
ooquistes con Ziehl-Neelsen o con inmunofluorescencia y la identificación de
antígenos por ELISA en materia fecal y se ha encontrado que todos tienen sensibilidad
y especificidad de 96% a 98%, por lo cual la escogencia depende de las
posibilidades de los laboratorios y de los costos de los reactivos.
En
biopsia intestinal se puede observar la atrofia de las vellosidades del
intestino y la hipertrofia de las criptas, en donde se localiza el parásito. Se
logran definir distintos estadios mediante las coloraciones comunes de hematoxilina
- eosina, en donde se ven de color violeta. También se usa la técnica de plata -
metenamina, Giemsa, Kinyoun y la inmunoperoxidasa. Es
posible también demostrar anticuerpos circulantes con inmunofluorescencia
indirecta y con técnicas de ELISA. En los estudios serológicos se consideran
significativos para el diagnóstico los títulos de 1:40 o superiores. Análisis
de alimentos y otras muestras: Investigación de ooquistes por microscopía, uso
de técnicas de biología molecular.
El tratamiento de base, apunta a un equilibrio del aporte hidroelectrolítico (reposición de pérdidas) y de nutrientes.
Se ha logrado una eficacia del 50 % en el tratamiento de los adultos con 2-3
g/día de espiromicina durante 7-30 días.
Las
medidas de prevención y control estarán basadas en las básicas para casi todas
las EPTA(s):
- Eliminación sanitaria de excretas.
- Provisión de agua segura (filtrada para eliminar partículas de 0,1-1 um).
- Educación para la salud.
- Los quistes son inactivados por calentamiento a temperatura de 72ºC durante un minuto o 45ºC durante 10-20 minutos o por congelación.
Cycloporiasis o Ciclosporiasis
(cie-10 a107.8)
Es
una enfermedad diarreica emergente con frecuencia en aumento, particularmente
en los meses de temperaturas cálidas. Fue descripta en 1977. Cyclospora
cayetanensis es
un parásito unicelular coccidio, de 8-10 µ de diámetro. La especie fue
designada en 1994, previamente se la denominó cianobacteria o cuerpo tipo
coccidio. Es
una de las parasitosis humanas que se descubrió recientemente, similar a
criptosporidiosis en su agente etiológico y en sintomatología. Cyclospora
cayetanensis (C. cayetanensis) es un protozoo patógeno emergente causante de
enfermedad diarreica. Esta coccidia era referida, por desconocerse su ubicación
taxonómica, como cuerpos similares a cyanobacteria o formas grandes de
Cryptosporidium.
Fue después de los estudios realizados por Ortega et al. que
se conoció su clasificación taxonómica. Estos investigadores después de inducir
la esporulación con solución de dicrómato de potasio a los conocidos como “cuerpos
similares a cyanobacterias” procedentes de casos clínicos, demostraron que el
microorganismo contenía por cada ooquiste, dos esporoquistes y dentro de cada
uno de ellos dos esporozoítos. Las características de los esporozoítos
observadas al microscopio electrónico mostraron organelos característicos de
los protozoos coccidias (Phylum Apicomplexa). Fue así como después de
identificar que pertenecían al género Cyclospora, se propuso la nomenclatura a
la especie como cayetanensis, por ser este el nombre de la Universidad de Lima,
Perú (Universidad Cayetano Heredia) donde se llevaron a cabo las
investigaciones.
Si
bien la infección por este parásito llamó la atención a la ciencia por estar
asociada a diarrea del viajero, adquirió una mayor relevancia en los primeros años
de la década de los 90, cuando se notifica su asociación con diarreas en
pacientes con Síndrome de Inmunodeficiencia Adquirida (SIDA). Adicionalmente, esta
coccidia comenzó a verse relacionada con la ingestión de frambuesas contaminadas. Cyclospora
spp.
afecta a animales y al hombre. Ha sido comunicada en numerosos países, siendo
más común en las regiones tropicales y subtropicales. Los ooquistes son
eliminados con las heces y esporulan en el medio ambiente en alrededor de dos
semanas a temperaturas de 22º a 32º C. La transmisión ocurre por la
contaminación fecal de agua y alimentos. La susceptibilidad es universal.
Han
ocurrido brotes internacionales, desde 1990, que afectaron aproximadamente a
3600 personas en los Estados Unidos y Canadá. Los alimentos fueron frambuesas
(procedentes de Guatemala), perejil y lechuga. Los brotes tienen un patrón
estacional con predominio en los meses cálidos.
Cyclospora
es un género en el Phylum Apicomplexa, de esta manera el parásito se relaciona
íntimamente con otros cuatro agentes biológicos dentro del grupo coccidias:
Cryptosporidium, Isospora, Toxoplasma y Sarcocystis. Se puede distinguir de
otras coccidias por su tamaño, forma y número de esporoquistes y esporozoítos. Los
ooquistes de C. cayetanensis, hasta el presente la única especie que se reporta
en el humano, son esféricos, con doble pared y miden de 8 a 10 μm de diámetro;
son algo más pequeños que los ooquistes de Cyclospora descritos en hospederos
no humanos. Al examinar las heces en fresco que contienen ooquistes de C.
cayetanensis, estos se ven como esferas hialinas (figura). En su interior presentan
una mórula de color verdoso con varios glóbulos refringentes que se disponen a
modo de racimo o roseta. Cuando esporula, en su interior se encuentran dos esporoquistes,
cada uno con dos esporozoítos. En heces viejas o preservadas, se ven pocos
glóbulos en su interior.
Como
los ooquistes de Cryptosporidium e Isospora, son ácido-alcohol resistentes. El
ciclo de vida de Cyclospora cayetanensis no ha sido totalmente dilucidado. La
presencia de ooquistes en heces sugiere que el ciclo sexual y el asexual pueden
desarrollarse en el hospedero humano. Su localización es intracitoplasmática,
dentro de una vacuola parasitófora en la región apical supranuclear de las
células epiteliales del intestino delgado; allí se reproduce y se multiplica.
Al salir al exterior con las heces los ooquistes no están esporulados.
Requieren de tiempo fuera del hospedero para su esporulación y convertirse en
infecciosos, por tanto la transmisión de persona a persona no es probable. El
tiempo requerido para la esporulación en la naturaleza no es conocido.
En
el laboratorio los microorganismos en condiciones óptimas de laboratorio
esporulan dentro de las primeras dos semanas de excretados. Se plantea que la
forma infectante llega a un nuevo hospedero susceptible a través del agua y los
alimentos contaminados. La
incidencia y prevalencia de la infección por Cyclospora cayetanensis se
desconocen, en parte por la pobre asistencia a las consultas médicas de las
personas con cuadros diarreicos, la poca sensibilidad de las técnicas
diagnósticas disponibles, el número reducido de ooquistes que aparece en las
heces del paciente, unido al poco uso de técnicas de concentración para protozoos
en los laboratorios, así como la poca indicación de realización de la técnica
de Ziehl-Neelsen y la inexperiencia de muchos de los laboratoristas para identificar
los ooquistes de Cyclospora.
Sin embargo, esta infección está siendo reportada en forma creciente en numerosos países a escala mundial, incluyendo Guatemala, Venezuela, Nueva Guinea, Cuba, Brasil, EUA, Canadá, Haití, Colombia y Turquía, Perú, Vietnam, Nepal, Egipto, entre otros. Esta información, en la mayor parte de las notificaciones, proviene de estudios realizados en viajeros internacionales, inmunodeprimidos y escolares.
Sin embargo, esta infección está siendo reportada en forma creciente en numerosos países a escala mundial, incluyendo Guatemala, Venezuela, Nueva Guinea, Cuba, Brasil, EUA, Canadá, Haití, Colombia y Turquía, Perú, Vietnam, Nepal, Egipto, entre otros. Esta información, en la mayor parte de las notificaciones, proviene de estudios realizados en viajeros internacionales, inmunodeprimidos y escolares.
En
el continente americano se han realizado múltiples reportes de esta infección.
En Guatemala, al estudiar personas de diferentes localidades se encontró que el
2,3% de la muestra estudiada, entre adultos y niños, estaban infectados por
esta coccidia. En Venezuela, entre la población indígena de San Antonio de
Morichal se encontró que entre las coccidias, esta fue la más prevalente
alcanzando hasta un 11,9%. En Cuba se encontró en un estudio en
inmunodeprimidos por SIDA que el 3% estaban infectados y en un estudio
realizado entre escolares de una zona urbana se demostró la presencia de
Cyclospora en 0,7% de los niños estudiados, algo menor de lo encontrado en
cuatro guarderías infantiles, donde se encontró un 1,5% de infectados. Cifras
superiores se encontraron entre niños ingresados en un hospital pediátrico,
donde el 3,7% de los ingresados en los servicios de atención a pacientes con
diarrea estaban infectados por este protozoo.
La
transmisión de persona a persona no ha sido documentada. Se reconoce que debe
pasar un tiempo fuera del hospedero, hasta el presente desconocido, para que
esporule y de esta forma sea infectante. Cyclospora
es transmitida por la ingestión de ooquistes esporulados, los cuales aparecen
como resultado de la contaminación fecal de las aguas y los alimentos. En un
brote hospitalario reportado en Chicago, la exposición a aguas contaminadas fue
implicada en la aparición de la enfermedad. Los ooquistes de Cyclospora son
probablemente, junto con los de otras coccidias, uno de los de más alta resistencia
a la desinfección por cloro.
La
posibilidad de la transmisión de Cyclospora por alimentos contaminados ha sido
comentada, basada en los datos epidemiológicos obtenidos durante diversas investigaciones
de brotes en los Estados Unidos de América y Canadá. Tres tipos de productos
frescos: frambuesas frescas, lechuga y albahaca han sido implicados como
vehículo de infección. Las frambuesas frescas importadas de Guatemala se han
asociado con brotes así como las congeladas a -3,3ºC.
Los
brotes de transmisión por alimentos resaltan la necesidad de fortalecer las
medidas de control y de prevención para asegurar que los productos alimentarios
que se comen crudos estén libres de Cyclospora cayetanensis, además de la
necesidad de continuar investigando sobre la biología y la epidemiología de esta
coccidia También se ha reportado la presencia de portadores sanos,
especialmente en países donde la infección es endémica.
La
influencia del clima en la infección ha sido vista en muchos países, a pesar de
los diferentes tipos de climas. Aunque se desconocen las causas, se piensa guarde
relación, en parte, a la fluctuación de temperatura y humedad. En Guatemala, en
un estudio hecho en un año de vigilancia a pacientes ambulatorios, mostró que
la infección era más frecuente en primavera, entre los niños de 1 a 9 años y en
las personas con gastroenteritis. En Turquía, fue más frecuente en el verano y
otoño. En la actualidad quedan muchas interrogantes sobre esta parasitosis
donde factores relacionados con Cyclospora cayetanensis, con el ambiente y con el
susceptible quedan por esclarecer.
Se
han encontrado ooquistes de Cyclospora en animales, principalmente reptiles y
roedores, que muy probablemente corresponden a otras especies diferentes a la
humana. C. cayetanensis se ha descrito en chimpancés. La mayoría de las
infecciones humanas se han encontrado en paí- ses en desarrollo o en personas
que han viajado a estos países, lo cual se explica por el alto riesgo de
contaminación fecal. La distribución geográfica es muy amplia y las
prevalencias varían de 2% a 18%. Estas cifras son más altas en personas con
diarrea. Se presentan brotes epidémicos en instituciones con deficiente
provisión de agua potable. El agua es considerada la principal fuente de
infección. Se describe un mayor número de casos en verano y en épocas de
sequía, cuando aumenta la contaminación hídrica.

La transmisión por manos es poco
probable, pues los ooquistes requieren un período de maduración en el agua o en
la tierra. Se presenta la infección en adultos y en niños inmunocompetentes y
se conocen abundantes casos en nmunodeficientes, principalmente en pacientes
con SIDA.
El período de incubación oscila de 1 a 7 días y estaría relacionado con la dosis inóculo. El período de estado es de comienzo brusco con: diarrea acuosa (seis o más evacuaciones/día), náuseas, vómitos, hiporexia, flatulencia, dolor cólico y distensión abdominal, hiporexia, fatiga, mialgias y pérdida de peso. Puede cursar con febricula o afebril. Dura de 9 a 43 días. Como complicaciones extraintestinales han sido comunicados síndrome de Guillain-Barré y síndrome de Reiter.
Después
de la exquistación del ooquiste de Cyclospora cayetanensis, los esporozoítos
invaden los enterocitos del intestino delgado (porción distal del duodeno y el
yeyuno), dentro de los cuales se reproducen sexual y asexualmente. Las formas asexuales
del parásito han sido encontradas en posición supranuclear dentro del citoplasma,
en las vacuolas parasitóforas. Ortega et al. en un estudio realizado en 17
pacientes observaron los gametocitos de este parásito por medio de microscopía óptica
y electrónica. Investigadores como Connor et al. han encontrado que en casos
asintomáticos la estructura histológica suele estar conservada. En casos
sintomáticos, junto a la presencia de diferentes estadios del parásito dentro
del enterocito, existen anomalías histológicas como el acortamiento de las
vellosidades intestinales y alteraciones celulares de los enterocitos, los que adquieren
forma columnar o cuboide; hay hiperplasia de las criptas y presencia de un
infiltrado inflamatorio de leucocitos polimorfonucleares, linfocitos y células plasmáticas
en la lámina propia. Muchos de los cambios inflamatorios pueden persistir, aún
después de que la infección cura.

La presencia de portadores sanos es frecuente, sobre todo en áreas endémicas. En los casos sintomáticos, después de un período de incubación promedio de 7 días, las personas infectadas por Cyclospora cayetanensis comienzan con un cuadro diarreico alto, caracterizado por un número entre 4 y 10 deposiciones diarias, acuosas, abundantes, con flema, pero sin sangre. También es frecuente encontrar dolores abdominales, nauseas, vómitos, anorexia, fatiga, flatulencia, pérdida de peso significativa y en un por ciento de los casos fiebre y escalofríos. Síntomas como mialgias y artralgias pueden preceder al cuadro diarreico. En general, las infecciones son autolimitadas en adultos sanos, pero pueden prolongarse en personas con determinado grado de compromiso inmunitario y aún sin este, resultando en una diarrea crónica asociada a nauseas, vómitos, dolor abdominal y anorexia.

El
diagnóstico de la infección por Cyclospora se sustenta al demostrar los
ooquistes en muestras de heces y ocasionalmente en aspirados duodenales. Los ooquistes
se ven como esferas de 8 a 10 μm de diámetro que contienen numerosos glóbulos
encerrados en su interior. Los ooquistes de Cyclospora autoflorescencomo
círculos azules cuando se examinan con un microscopio de fluorescencia
ultravioleta ajustado con un filtro de excitación de 365nm. Esta propiedad no es
específica para Cyclospora y disminuye con el tiempo de la muestra.


El
examen de las heces frescas por el método directo con Solución de Lugol
parasitológico pone al descubierto la presencia de esta infección. En muchos pacientes
en los que sólo aparece un número reducido de microorganismos, se impone
entonces hacer uso de las técnicas de concentración como la de Ritchie y lade
Sheater.
Al
igual que los ooquistes de Cryptosporidium e Isospora, los ooquistes de
Cyclospora son ácidoalcohol resistente; por ello la técnica de Ziehl-Neelsen modificada
y la coloración de Kinyoun son de utilidad para revelar la presencia.

Hasta el presente, la única droga que se muestra como tratamiento de elección para la infección por C. cayetanensis es el trimetoprim-sulfametoxazol (TMP-SMX), el que provoca la mejoría clínica y la erradicación del parásito en un alto porcentaje de los casos. La dosificación propuesta para los adultos ha sido (160/800mg) tomado 2 veces al día durante 7 a 10 días. Evaluar el equilibrio hidromineral y ácido básico del paciente también debe considerarse en casos de diarrea por Cyclospora cayetanensis. Fármacos como la norfloxacina, el tinidazol, la quinacrina, el ácido nalidíxico, el furoato de diloxanida, el metronidazol, la azitromicina y el albendazol han sido evaluados y no parecen ser efectivos.
Hasta el presente, la única droga que se muestra como tratamiento de elección para la infección por C. cayetanensis es el trimetoprim-sulfametoxazol (TMP-SMX), el que provoca la mejoría clínica y la erradicación del parásito en un alto porcentaje de los casos. La dosificación propuesta para los adultos ha sido (160/800mg) tomado 2 veces al día durante 7 a 10 días. Evaluar el equilibrio hidromineral y ácido básico del paciente también debe considerarse en casos de diarrea por Cyclospora cayetanensis. Fármacos como la norfloxacina, el tinidazol, la quinacrina, el ácido nalidíxico, el furoato de diloxanida, el metronidazol, la azitromicina y el albendazol han sido evaluados y no parecen ser efectivos.
Las medidas de prevención contra esta infección aún quedan por ser establecidas. Para prevenir la exposición la filtración parece ser un método útil, al permitir eliminar los ooquistes del agua, basándose en su tamaño; también resulta seguro hervir el agua para beber. En cambio, se sabe que este parásito es resistente a la cloración. En cuanto a los alimentos que se consumen crudos, en Perú, en un estudio en el que se tomaron muestras de vegetales en algunos mercados durante las estaciones de alta incidencia, al final de esta estación y durante la estación de baja incidencia, se demostró que aún lavando los vegetales los ooquistes de Cyclospora no eran posibles de eliminar por completo.
"SOMOS
LO QUE HACEMOS REPETIDAMENTE. EXCELENCIA, POR LO TANTO, NO ES UN ACTO SINO UN
HABITO" - ARISTOTELES


Comentarios
Publicar un comentario